**锂亚硫酰氯 (Li-SOCl2) 电池原理**
锂亚硫酰氯 (Li-SOCl2) 电池是一种一次(不可充电)电池,以其高能量密度、长保质期和宽工作温度范围而闻名。它们通常用于可靠性、寿命和功率密度至关重要的应用,例如远程传感器、医疗设备和军事设备。
**工作原理**
锂亚硫酰氯 (Li-SOCl2) 电池的工作原理是基于锂金属 (Li) 和亚硫酰氯 (SOCl2)(液态非水电解质)之间的电化学反应。该反应涉及锂离子和电子在电池阳极(锂金属)和阴极(亚硫酰氯)之间的转移。
总体反应如下:
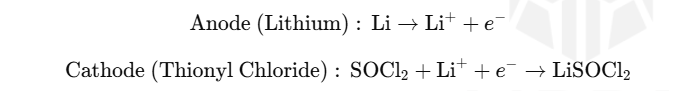
**关键组件**
1. **阳极(锂金属)**:
- 阳极由高纯度锂金属制成,作为锂离子的来源。放电过程中,阳极中的锂金属发生氧化(失去电子),释放出锂离子 (Li⁺)。
2. **阴极(亚硫酰氯)**:
- 阴极由亚硫酰氯 (SOCl2) 组成,在放电过程中发生还原(获得电子)。锂离子 (Li+) 从阳极迁移并与亚硫酰氯反应,形成锂亚硫酰氯 (LiSOCl2)。
3. **电解质**:
- Li-SOCl2 电池中的电解质通常是溶解在亚硫酰氯中的锂盐(例如四氯铝酸锂,LiAlCl4)溶液。这种电解质促进锂离子在阳极和阴极之间的移动,从而发生电化学反应。
4. **分隔符**:
- 在阳极和阴极之间放置隔膜,以防止短路,同时允许离子通过。
**放电过程**
1. **在阳极(锂金属)**:
- 阳极中的锂金属失去电子并变成锂离子(Li⁺)。这些锂离子通过电解质迁移到阴极。
- **阳极反应**:
Li→Li++e−
2. **在阴极(亚硫酰氯)**:
- 来自阳极的锂离子 (Li⁺) 与流经外部电路的电子一起在阴极与亚硫酰氯 (SOCl2) 发生反应,形成锂亚硫酰氯 (LiSOCl2)。
- **阴极反应**:
SOCl2+Li++e−→LiSOCl2
阳极氧化反应期间释放的电子流过外部电路,为设备提供电力。
**整体反应**
锂亚硫酰氯电池中的总体电化学反应为:
Li+SOCl2→LiSOCl2
**锂亚硫酰氯电池的优点**
1. **高能量密度**:
- 锂亚硫酰氯电池具有非常高的能量密度,这使得它们非常适合需要小尺寸持久电力的应用。
2. **保质期长**:
- 由于亚硫酰氯的稳定化学性质和电池的不可充电特性,Li-SOCl2 电池即使在不使用时也可以持续使用多年而不会出现明显退化。
3. **宽温度范围**:
- 这些电池在 -60°C 至 +85°C 的广泛温度范围内表现良好,适合在恶劣环境中使用。
4. **低自放电率**:
- 锂亚硫酰氯电池的自放电率非常低,这意味着即使存放数年,它们也能长时间保持电量。
5. **高电压**:
- 这些电池提供相对较高的标称电压(通常约为 3.6V),可用于为各种电子设备供电。
**应用**
锂亚硫酰氯电池通常用于需要长期可靠电力的应用,包括:
- **远程传感器**:用于气象站、环境监测和其他遥感设备。
- **医疗设备**:常见于起搏器、助听器和其他需要持久、可靠电源的医疗植入物。
- **军事和航空航天**:用于需要长保质期和高能量密度的设备,例如应急信标和卫星设备。
- **公用事业计量**:用于燃气、水和电力监控的智能仪表。
- **消费电子**:在摄像头、安全系统和备份系统等设备中。
**缺点**
1. **毒性**:
- 亚硫酰氯是一种有毒和腐蚀性物质,因此正确处理和处置这些电池对于避免环境危害至关重要。
2. **不可充电**:
- Li-SOCl2 电池是原电池,这意味着它们不可充电。一旦耗尽,必须妥善处置和更换。
3. **成本**:
- 由于使用的材料和复杂的制造工艺,这些电池往往比其他类型的原电池(如碱性电池)更昂贵。
---
**结论**
锂亚硫酰氯 (Li-SOCl2) 电池的工作原理是锂金属和亚硫酰氯之间的电化学反应。它们具有能量密度高、保质期长和工作温度范围宽等优点,非常适合需要可靠、长期供电的应用。然而,它们的毒性和不可充电的性质需要小心处理和处置。
